镀锡镀液中铅离子沉淀及控制技术研究
[关键词:镀锡,铅离子,沉淀控制] [热度 ]| 提示:此毕业设计论文完整版包含【论文,答辩稿】 作品编号:clkx0025,word全文:37页,合计:17000字 |

设计(论文)的基本内容:
通过化学沉淀法研究了苯酚磺酸(PSA)体系下镀液除铅效果,并分析了镀液温度和静置时间对除铅效果的影响。通过原子吸收光谱(AAS)技术分析电镀液中 Pb 离子的含量,采用 X 射线衍射(XRD)对沉淀物进行物相分析,并进一步对不同物质除铅机理进行分析和推测。
本实验通过化学沉淀法研究了苯酚磺酸(PSA)体系下镀液除铅效果,并分析了镀液温度和静置时间对除铅效果的影响。通过原子吸收光谱(AAS)技术分析电镀液中 Pb 离子的含量,采用 X 射线衍射(XRD)对沉淀物进行物相分析,并进一步对不同物质除铅机理进行分析和推测。
氢氧化钡、碳酸钡除铅效果显著。当镀液中加入 0.5g/L 的碳酸锶,残液中铅离子含量大幅降低,但浓度依然较高。在一定温度范围内,铅离子含量随着温度的升高而降低, 当温度继续升高至 60℃时,除铅效果反而略有降低。随着陈化时间的增加,沉淀吸附反应后镀液中残留的铅离子在逐渐降低。
镀液中加入 Ba(OH)2、BaCO3 反应后,所得共沉淀物均为 Pb2+取代 Ba2+形成取代固溶体(Ba, Pb)SO4。添加 SrCO3 反应后所得的沉淀物为 SrSO4。
本文研究内容及目的
苯酚磺酸(PSA)镀液体系由于生产效率高、生产陈本低、产品性能优良等特点, 被广泛应用于镀锡板的生产。但在镀锡板工业生产中使用的锡含有微量的 Pb,在电镀过程导致锡液中含有微量杂质 Pb,Pb 与 Sn 为第Ⅳ族元素,性质相近,标准电极电势比较接近(Pb:﹣0.126V,Sn:﹣0.136V),在电镀过程中极易产生共沉积。因此除去镀液中的铅成为了实际生产中一个迫切的问题。
化学上传统处理溶液中铅的主要方法是沉淀法。针对本文镀液中 Pb2+的环境特点, 通过分析与总结,主要进行以下研究:
(1)使用化学分析纯的氢氧化钡、碳酸钡、碳酸锶进行除铅试验。通过对比来分析不同浓度试剂的除铅效果。
(2)通过以上实验分析得到最佳的除铅试剂,然后分析不同工艺条件(温度、静置时间)对镀液中除铅效果影响。
(3)收集镀液中加入氢氧化钡、碳酸钡、碳酸锶后所得的沉淀,进行物相分析,从而进一步研究加入沉淀剂时的反应机理。
1.在同等条件,且试剂均为足量(3g/L)的时候,仅看除铅效果,碳酸锶除铅效果最好,碳酸钡与氢氧化钡除铅效果较好且相近。在少量试剂(0.5g/L)的情况下,碳酸钡与氢氧化钡有明显除铅效果。但实际生产中,碳酸锶价格为氢氧化钡、碳酸钡的二倍, 碳酸钡与氢氧化钡效果相近,但碳酸根离子与镀液中游离酸反应剧烈,并产生大量 CO2 气体,故在实际中建议使用氢氧化钡。
2.由于温度对于反应的促进作用,在一定温度范围内,铅离子含量随着温度的升高而降低。但升高至 60℃以上时,铅离子含量反而升高,推测是由于在更高温度下,由吸附而沉淀下来的铅离子很容易再度扩散到溶液当中,使除铅效果降低。
3.随着陈化时间的增加,沉淀吸附反应后镀液中残留的铅离子在逐渐降低。但是由实验可以看到,只有长时间陈化才有明显效果,故在实际生产中效果不明显。
4.镀液中加入 Ba(OH)2 反应后,所得共沉淀物为 Pb2+取代 Ba2+形成取代固溶体
(Ba, Pb)SO4,不含有 PbSO4。镀液中加入 BaCO3 后,反应激烈,瞬间产生大量的 CO2气体,所得沉淀为(Ba, Pb)SO4。添加 SrCO3 反应后所得的沉淀物为 SrSO4。

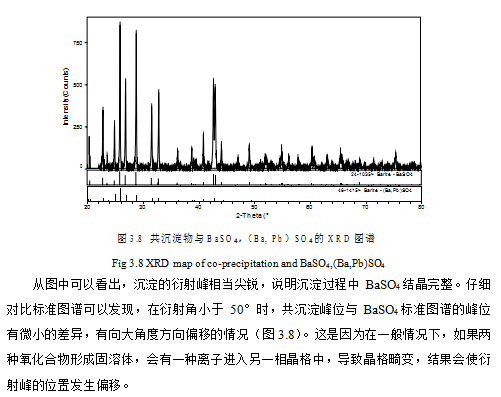
| 提示:此毕业设计论文完整版包含【论文,答辩稿】 作品编号:clkx0025,word全文:37页,合计:17000字 |
本材料科学与工程毕业设计论文作品由 毕业论文设计参考 [http://www.qflunwen.com] 征集整理——镀锡镀液中铅离子沉淀及控制技术研究(论文,答辩稿)!
-
没有关键字相关信息!

 当前位置:
当前位置: 